Este vídeo rodado con la técnica time-lapse es una de las más convincentes, e inquietantes, visualizaciones de la evolución que hemos visto nunca. Las imágenes presentan una cepa de la bacteria intestinal E. coli en plena evolución hasta volverse, por sus propios medios, 1.000 veces más resistente a un antibiótico en cuestión de 11 días, mostrando de una manera totalmente cruda la velocidad con la que las enfermedades se pueden adaptar a las drogas que arrojamos en su camino.
Esta sorprendente demostración sucede en una placa de Petri gigante llamada “la placa de Evolución Microbiana y Patio de Crecimiento (MEGA-placa, por sus siglas en inglés), pero los investigadores que la diseñaron rehúsan atribuirse el mérito de ella. «Realmente no inventamos la MEGA-placa. Si acaso, fue inventada en Hollywood», dice Roy Kishony, un biólogo de sistemas en el Instituto de Tecnología Technion-Israel. «No sé si conoces la película Contagio, pero tiene una valla publicitaria que fue hecha para ella, y es básicamente una gigantesca placa de Petri», dice.
El cartel de Contagio le dio a Kishony una idea. Si él y su compañero de equipo, que incluía a los biólogos de Harvard Tami Lieberman y Michael Baym, pudieran construir una placa de Petri lo suficientemente grande, podrían utilizarla para visualizar la resistencia a los antibióticos de una manera lúcida. No es ningún secreto que las superbacterias resistentes a los medicamentos están haciendo cada vez más difícil el tratamiento de todo tipo de condiciones desde la gonorrea hasta las infecciones del tracto urinario, y la evidencia sugiere que la amenaza es probable que aumente. Pero la resistencia a los antibióticos es un problema difícil de visualizar, y no sólo porque las bacterias son organismos microscópicos. La resistencia adquirida es un concepto que puede ser difícil de convencer a los no científicos que, obviamente, cuentan con una formación específica más limitada. Hablamos sobre los antibióticos y la resistencia que están desarrollando en nuestra historia «¿Qué es la penicilina; cómo se descubrió; terminará su efecto?» que puedes leer aquí.
Así Kishony y su equipo construyeron la MEGA-placa y la llenaron con un soporte en el que el E. coli pudiera crecer, morir, evolucionar, y propagarse. A continuación dosifican el medio con concentraciones cada vez mayores de antibióticos; los extremos opuestos de la placa no recibieron ningún antibiótico en absoluto, pero para cuando alcanzaron el centro de la placa, Kishony y su equipo habían incrementado la dosis de antibióticos a 1000 veces la concentración necesaria para matar a su cepa inicial de E. coli. Tras esto, encendieron su cámara de vídeo, depositaron la sección libre de antibióticos de la placa con las bacterias, y observaron lo que sucedía.
Requirió un poco de trabajo (las primeras colonias sucumbieron a la contaminación y la condensación de agua) pero con el tiempo, consiguieron el vídeo que te mostramos. «De repente se convirtió en algo mágico», dice Kishony. El vídeo es un time-lapse a lo largo de 11 días. Cada segundo de vídeo se traduce en alrededor de cinco horas de tiempo real.
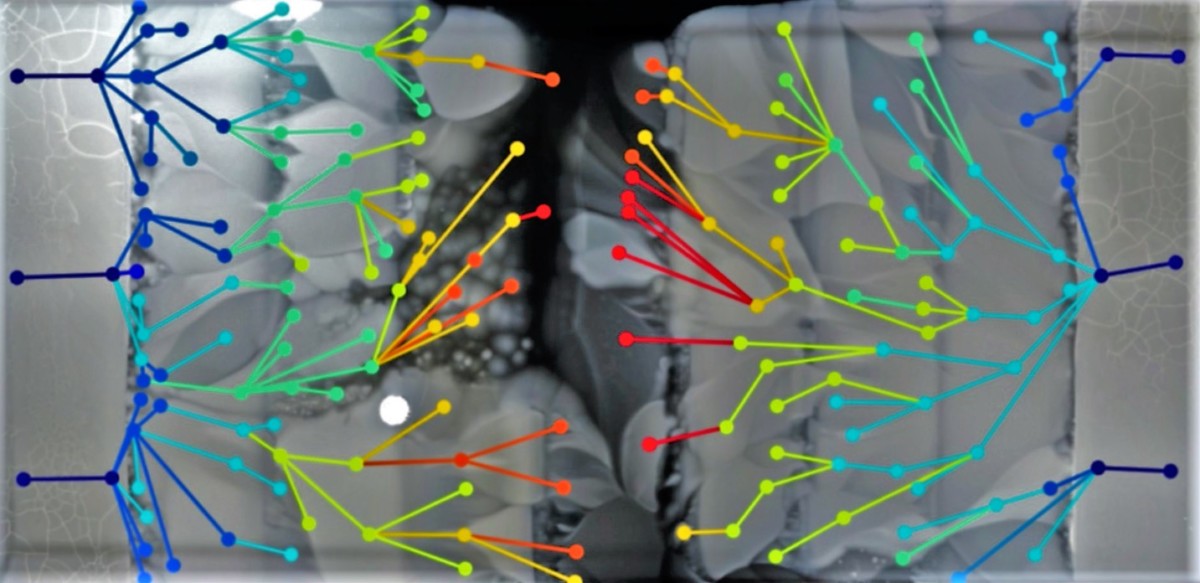
En él, se puede ver como la colonia bacteriana se propaga, blanca y con apariencia espumosa, a través del agar en la placa de Petri. Conforme la colonia se encuentra con una mayor concentración de antibiótico, se detiene. Las bacterias que no están preparadas perecen. Pero segundos después, una pequeña extensión de la colonia cruza el umbral. Estos microbios pioneros, que han desarrollado resistencia a la mayor concentración de antibiótico, van a colonizar este nuevo territorio, impregnado con mayor dosis de antibiótico, hasta que se encuentran con el siguiente límite antibacteriano. El proceso entonces se repite. En cada nueva etapa, bacterias mutantes cruzan el umbral y se lanzan hacia adelante, engendrando a su paso una cepa cada vez más resistentes de E. coli.
Kishony y su equipo sabían que esto iba a pasar, pero eso no significa que la MEGA-placa carezca de sentido. Para empezar, es una visualización muy elocuente y poco común de la evolución y su papel en el surgimiento de las superbacterias. También da a los biólogos una herramienta para analizar mejor cómo se desarrollan estas superbacterias. Tal y como suena, este video es el primero de muchos. «Estamos pensando en identificar todas las maneras que tienen las diferentes bacterias de volverse resistentes, y utilizar esto para desarrollar herramientas de diagnóstico que puedan prever el futuro,» dice Kishony. Con eso, los médicos pueden aprender más acerca de cómo estos patógenos evolucionan, y lo que pueden hacer para detenerlos.
Traducción del vídeo: Así que lo que terminamos contruyendo fue, básicamente, una placa de Petri, solo que de 2 por 4 pies, y la manera en que la dispusimos es a través de 9 bandas y al final de cada una de estas bandas colocamos un agar de espesor común a las placas de Petri con diferentes cantidades de antibiótico. En los extremos no hay antibiótico; junto a ellos, hay apenas un poco más de lo que necesita el E. coli para sobrevivir; junto a esto, hay diez veces más, luego 100 veces; y entonces, finalmente la banda central contiene 1.000 veces mayor cantidad de antibiótico. Entonces, por encima de ellos vertemos un fino agar que permite el movimiento de las bacterias. El fondo es negro porque contiene tinta, y las bacterias aparecen en blanco. Primero se observa cómo las bacterias se expanden por la zona sin antibiótico hasta llegar a un punto donde ya no pueden sobrevivir. Entonces un mutante aparece a la derecha. Es resistente a los antibióticos. Se extiende hasta que comienza a competir con otros mutantes de su entorno. Cuando estos mutantes llegan al siguiente límite, ellas también se tienen que detener y desarrollar nuevas mutaciones para poder llegar a la zona con 10 veces más antibiótico. Entonces puedes ver los diferentes mutantes repetir esto con 100 veces más antibiótico, y después de unos 11 días, finalmente consiguen llegar a la zona con 1.000 veces la cantidad de antibiótico límite para la supervivencia de la bacteria salvaje. Y de este modo podemos ver tras este proceso de acumular mutaciones sucesivas que la bacteria que es generalmente sensible a un antibiótico puede desarrollar resistencia a concentraciones extremadamente altas en un periodo de tiempo corto.